Les liquides sont un état condensé : le volume d’un liquide ne change pas beaucoup quand une pression est appliquée. Un liquide est un fluide : il n’a pas sa propre forme et les molécules peuvent se déplacer à l’intérieur. Comme dit précédemment les liquides sont caractérisés par un ordre à courte portée et un désordre à longue portée.
Propriétés des liquides :
1) La tension superficielle :
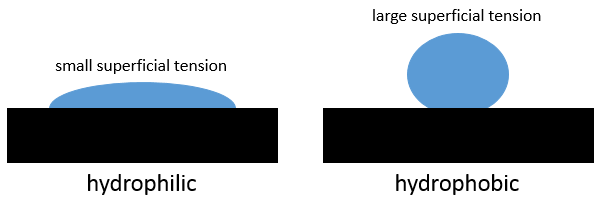
Quand une goutte d’eau tombe sur une surface métallique (par exemple), la gouttelette ne se propage pas complètement. La goutte n’est pas une monocouche de l’eau mais a encore une forme caractéristique et une largeur :
La forme dépend des interactions entre les molécules du liquide, entre elles, et de leur interaction avec les molécules de la surface. Si les interactions avec la surface sont plus fortes que les interactions internes du liquide alors la goutte se propage sur la surface. La surface est dite hydrophile si un liquide se répand sur elle. A l’opposé, sur une surface hydrophobe, les gouttelettes restent dans une forme sphérique (il est possible d’avoir presqu’ une sphère complète). Si la surface est inclinée la gouttelette va simplement rouler sur la surface. Avec une surface inclinée spécialement conçue en forme d’escalier , il est possible pour une gouttelette de grimper sur elle (Enhanced Droplet Contrôle par ébullition de transition, Alex Grounds, Richard Still & Kei Takashina, rapports scientifiques 2, 720)
La tension superficielle est une propriété du liquide tandis que l’hydrophobie est une propriété de la surface.
Pour augmenter la surface (par ΔS), entre un liquide et un solide, un travail W est nécessaire :
γ est donné pour un type de surface de sorte qu’il ne dépend que de l’interaction entre les molécules du liquide. Une petite tension superficielle signifie que le liquide se propage facilement, que le travail pour augmenter sa surface avec le solide est petite. Par exemple l’huile se répand facilement sur une surface. Au contraire le mercure a des liaisons métalliques très fortes et minimise sa surface avec le solide, il garde une forme sphérique.
2) La Capillarité :
C’est la capacité d’un liquide à circuler dans les espaces étroits sans forces extérieures ou à l’encontre de forces extérieures. Typiquement, si vous plongez partiellement un morceau de papier dans l’eau, l’eau se déplace vers le haut sur le papier en dépit de l’influence de la gravité. La capillarité est la résultante de plusieurs forces : la force d’adhésion entre le liquide et la surface contre le poids du liquide et la force de cohésion dans le liquide. Sur le papier, l’eau va arrêter de se déplacer vers le haut lorsque les forces s’ annulent entre elles :
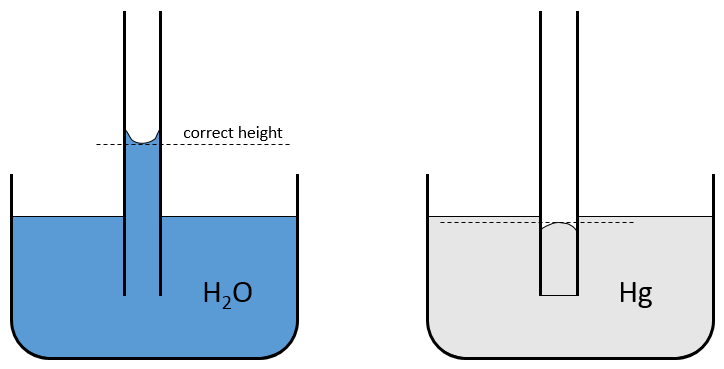
Dans un tube de verre la force d’adhésion est importante parce que le verre possède des anions O- qui favorisent l’adhérence. Par conséquent la plupart des liquides inorganiques vont grimper dans un tube, nous pouvons voir que la surface du liquide n’est généralement pas plat mais est plutot incurvée, il est appelé le ménisque. L’énergie d’adhésion est suffisamment favorable pour augmenter légèrement la surface de l’eau-air de sorte que la hauteur le long de la paroi est supérieure par rapport au milieu du tube. La différence de hauteur peut être de plusieurs millimètres. Sur un tube gradué la hauteur à considérer est celle du milieu du tube.
Lorsque la force d’adhésion est inférieure à la force de cohésion, le niveau dans le tube sera plus faible que le niveau du liquide hors de celui-ci, c’est le cas pour le mercure. Son ménisque est également différent de la surface du bain de l’eau comme le mercure évite le contact avec la surface.